Europij, simbol je Eu, a atomski broj je 63. Kao tipičan član lantanoida, europij obično ima valenciju +3, ali je česta i valencija kisika +2. Postoji manje spojeva europija s valentnim stanjem +2. U usporedbi s drugim teškim metalima, europij nema značajne biološke učinke i relativno je netoksičan. Većina primjena europija koristi učinak fosforescencije europijevih spojeva. Europij je jedan od najmanje zastupljenih elemenata u svemiru; u svemiru postoji samo oko 5 × 10-8% tvari.
Europij se nalazi u monazitu
Otkriće europija
Priča počinje krajem 19. stoljeća: u to vrijeme, izvrsni znanstvenici počeli su sustavno popunjavati preostala praznine u Mendeljejevljevom periodnom sustavu elemenata analizirajući spektar atomske emisije. U današnjem smislu, taj posao nije težak i može ga dovršiti i student preddiplomskog studija; ali u to vrijeme, znanstvenici su imali samo instrumente niske preciznosti i uzorke koje je bilo teško pročistiti. Stoga su tijekom cijele povijesti otkrića lantanoida svi „kvazi“ otkrivači stalno iznosili lažne tvrdnje i međusobno se prepirali.
Godine 1885. Sir William Crookes otkrio je prvi, ali ne baš jasan signal elementa 63: u uzorku samarija uočio je specifičnu crvenu spektralnu liniju (609 nm). Između 1892. i 1893. godine, otkrivač galija, samarija i disprozija, Paul é mile LeCoq de Boisbaudran, potvrdio je ovu vrpcu i otkrio još jednu zelenu vrpcu (535 nm).
Zatim je 1896. godine Eugène Anatole Demar strpljivo odvojio samarijev oksid i potvrdio otkriće novog rijetkog zemnog elementa koji se nalazi između samarija i gadolinija. Uspješno je odvojio ovaj element 1901. godine, označivši kraj otkrića: „Nadam se da ću ovaj novi element nazvati Europij, sa simbolom Eu i atomskom masom od oko 151.“
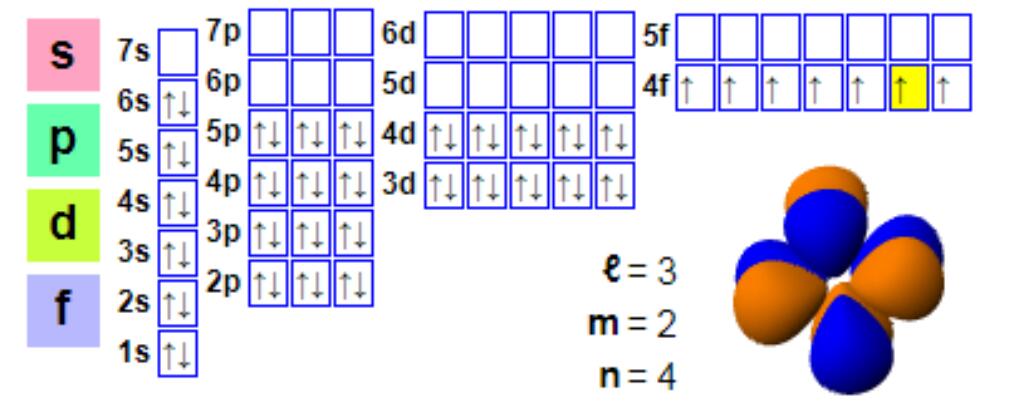
Elektronska konfiguracija
Elektronska konfiguracija:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
Iako je europij obično trovalentan, sklon je stvaranju dvovalentnih spojeva. Ovaj fenomen razlikuje se od stvaranja spojeva s +3 valencijom većine lantanoida. Dvovalentni europij ima elektroničku konfiguraciju 4f7, jer poluispunjena f ljuska pruža veću stabilnost, a europij (II) i barij (II) su slični. Dvovalentni europij je blago redukcijsko sredstvo koje oksidira na zraku stvarajući spoj europija (III). U anaerobnim uvjetima, posebno uvjetima zagrijavanja, dvovalentni europij je dovoljno stabilan i sklon je ugradnji u kalcij i druge zemnoalkalijske minerale. Ovaj proces ionske izmjene osnova je „negativne anomalije europija“, odnosno, u usporedbi s obiljem hondrita, mnogi lantanoidni minerali poput monazita imaju nizak sadržaj europija. U usporedbi s monazitom, bastnezit često pokazuje manje negativnih anomalija europija, pa je bastnezit također glavni izvor europija.
Europij je željezno sivi metal s talištem od 822 °C, vrelištem od 1597 °C i gustoćom od 5,2434 g/cm³. To je najmanje gusti, najmekši i najhlapljiviji element među rijetkozemnim elementima. Europij je najaktivniji metal među rijetkozemnim elementima: na sobnoj temperaturi odmah gubi svoj metalni sjaj na zraku i brzo oksidira u prah; Burno reagira s hladnom vodom stvarajući vodik; Europij može reagirati s borom, ugljikom, sumporom, fosforom, vodikom, dušikom itd.
Primjena europija
Europijev sulfat emitira crvenu fluorescenciju pod ultraljubičastim svjetlom
Georges Urbain, mladi izvanredni kemičar, naslijedio je spektroskopski instrument Demarçaya i otkrio da uzorak itrijevog(III) oksida dopiranog europijem emitira vrlo jarku crvenu svjetlost 1906. godine. To je početak dugog putovanja europijevih fosforescentnih materijala – koji se ne koriste samo za emitiranje crvene svjetlosti, već i plave svjetlosti, jer emisijski spektar Eu2+ spada u to područje.
Fosfor sastavljen od crvenih Eu3+, zelenih Tb3+ i plavih Eu2+ emitera ili njihove kombinacije može pretvoriti ultraljubičasto svjetlo u vidljivo svjetlo. Ovi materijali igraju važnu ulogu u raznim instrumentima diljem svijeta: zaslonima za pojačavanje X-zraka, katodnim cijevima ili plazma zaslonima, kao i novijim energetski štedljivim fluorescentnim žaruljama i svjetlećim diodama.
Fluorescentni učinak trovalentnog europija može se senzibilizirati i organskim aromatskim molekulama, a takvi se kompleksi mogu primijeniti u raznim situacijama koje zahtijevaju visoku osjetljivost, poput tinti protiv krivotvorenja i barkodova.
Od 1980-ih, europij igra vodeću ulogu u visoko osjetljivim biofarmaceutskim analizama korištenjem vremenski razlučene metode hladne fluorescencije. U većini bolnica i medicinskih laboratorija takva je analiza postala rutina. U istraživanjima znanosti o životu, uključujući biološko snimanje, fluorescentne biološke sonde izrađene od europija i drugih lantanoida su sveprisutne. Srećom, jedan kilogram europija dovoljan je za potporu otprilike milijardu analiza - nakon što je kineska vlada nedavno ograničila izvoz rijetkih zemalja, industrijalizirane zemlje u panici zbog nedostatka skladišta rijetkih zemalja ne moraju se brinuti o sličnim prijetnjama takvim primjenama.
Europijev oksid se koristi kao fosfor sa stimuliranom emisijom u novom rendgenskom medicinskom dijagnostičkom sustavu. Europijev oksid se također može koristiti za proizvodnju obojenih leća i optoelektroničkih filtera, za uređaje za pohranu magnetskih mjehurića te u kontrolnim materijalima, zaštitnim materijalima i strukturnim materijalima atomskih reaktora. Budući da njegovi atomi mogu apsorbirati više neutrona od bilo kojeg drugog elementa, često se koristi kao materijal za apsorpciju neutrona u atomskim reaktorima.
U današnjem brzo rastućem svijetu, nedavno otkrivena primjena europija mogla bi imati dubok utjecaj na poljoprivredu. Znanstvenici su otkrili da plastika dopirana dvovalentnim europijem i jednovalentnim bakrom može učinkovito pretvoriti ultraljubičasti dio sunčeve svjetlosti u vidljivu svjetlost. Ovaj proces je prilično zelen (to su komplementarne boje crvene). Korištenje ove vrste plastike za izgradnju staklenika može omogućiti biljkama da apsorbiraju više vidljive svjetlosti i povećaju prinos usjeva za otprilike 10%.
Europij se također može primijeniti na kvantne memorijske čipove, koji mogu pouzdano pohranjivati informacije nekoliko dana u komadu. To može omogućiti pohranu osjetljivih kvantnih podataka u uređaj sličan tvrdom disku i njihovu dostavu diljem zemlje.
Vrijeme objave: 27. lipnja 2023.